Žiadne produkty
Ceny sú s DPH
Kategórie
- Ponuka práce: FARMACEUT - LEKÁRNIK
- K O R O N A V Í R U S - COVID-19
- Plus lekáreň
- Ambulancia lekára
- Bandáže, návleky, pásy
- Barle, palice, chodítka
- Bylinné prípravky
- Dezinfekcia
- Diagnostické testy
- Elektro
- Glukometer
- Iné pomôcky pre pacientov
- Inhalátory
- Inkontinencia - únik moču
- Invalidita
- Kompresívna liečba
-
Kozmetika - Drogéria
- Telová kozmetika
- Vlasová kozmetika
- Pleťová kozmetika
- Prípravky na holenie a depiláciu
- Intímna hygiena
- Pranie
- Domácnosť
-
Značky
- Himalaya
- Adidas
- Airwick
- Ajax
- Alex
- Always
- Ambipur
- Ariel
- Aussie
- Axe
- Batiste
- Bel
- Bonux
- Bref
- Bubchen
- Calgon
- Cif
- Cilit Bang
- Clin
- Coccolino
- Denim
- Dettol
- Discreet
- Domestos
- Dove
- Duck
- Durex
- Elseve
- Eos
- Fa
- Finish
- Fixinela
- Garnier
- Gillette
- Glade
- Got2be
- Head & Shoulders
- Jar
- Johnsons
- Kallos
- Kleenex
- Kneipp
- Ko+ex
- Lanza
- Lenor
- Loreal
- Mexx
- Mr. Proper
- Naturella
- Neutrogena
- Nivea
- Nova Car Care
- o.b.
- Old Spice
- Oral -B
- Palette
- Palmolive
- Pampers
- Pantene
- Persil
- Perwoll
- Playboy
- Pronto
- Puella
- Pur
- Raid
- Rex
- Rexona
- Ria
- Sanytol
- Savo
- Schauma
- Scholl
- Signal
- Silan
- Somat
- STR8
- Syoss
- Taft
- Tesori d-oriente
- TRESemmé
- Vanish
- Veet
- Wella
- Wilkinson
- Woolite
- Zewa
- Starostlivosť o vlasy
- Lekárničky, náplne
- Liečba svetlom
- Masážne prípravky
- Mikroskopy
- Opaľovanie
- Optické prístroje špeciálne
- Pečené čaje z ovocia
- Potravinové doplnky
- Pre dámy
- Pre deti
- Pre pánov
- Preležaniny a ošetrovanie
- Repelenty
- Starostlivosť o nechty
- Starostlivosť o nohy
- STÓMIA a stomické pomôcky
- Teplomery
- Tlakomery
- Veterinárne liečivá
-
Voľnopredajné lieky
- Alergia
- Antikoncepcia
- Bolesť hlavy
- Bolesť hrdla
- Bolesť svalov a kĺbov
- Bolesti zubov
- Chrípka a prechladnutie
- Dezinfekcia kože
- Fytofarmaká
- Homeopatiká
- Horúčka
- Horúčka u detí
- Imunitný systém
- Intímna hygiena
- Kašeľ
- Kožné choroby
- Kŕčové žily
- Krv, srdce a obehový systém
- Menštruačné bolesti
- Na chudnutie
- Poruchy trávenia
- Spánok
- Stop fajčeniu
- Upchatý nos
- Vlasy, nechty pokožka
- Výživové doplnky
- Urologické problémy
- Zmyslové orgány
- Pamäť a normálná funkciá nervovej sústavy
-
Voľnopredajné lieky podľa skupín
- 69 - Otorinolaringologiká
- 24 - Antihistaminiká, histamín
- 46 - Dermatologiká
- 17 - Antikoncepčné prípravky
- 07 - Analgetiká, antipyretiká
- 29 - Antireumatiká, antiflogistiká, antiuratiká
- 86 - Vitamíny, vitagény
- 52 - Expektoranciá, mukolytiká
- 93 - Homeopatiká
- 94 - Fytofarmaká
- 15 - Antibiotiká (proti mikróbom a vírusovým infekciám)
- 39 - Soli a ióny pre perorálnu a perenterálnu aplikáciu
- 70 - Anxiolytiká
- 85 - Venofarmaká, vazoprotektíva
- 87 - Varia I
- 95 - Stomatologiká III
- 49 - Digestíva, adsorbenciá, acidá
- 32 - Antiseptiká, dezinficienciá (lokálne)
- 92 - Tradičný rastlinný liek
- 91 - Multivitamíny a stopové prvky
- 54 - Gynekologiká
- 36 - Antitusiká
- 26 - Antimykotiká (lokálne a celkové)
- 42 - Chemoterapeutiká (vrátane tuberkulostatík)
- 23 - Antihemoroidiká
- 16 - Antikoagulanciá (fibrinolytiká, antifibrinolytiká)
- 41 - Kardiaká
- 12 - Antianemiká
- 61 - Laxatíva
- 43 - Choleretiká, cholekinetiká
- 09 - Antacidá (vrátane antiulceróznych liečiv)
- 20 - Antiemetiká, antikinetiká
- 73 - Spazmolytiká
- Výživové nápoje
- Zdravé zuby
- Všeobecná ambulancia pre dospelých, körzeti orvosi rendelö MUDr. Rudolf Pelikán
- Zdravotná obuv ktorá pomáha
- Gynekologicko - pôrodnícka ambulancia
- NANO produkty
- Naši partneri
- Záhrada
- Lekáreň TABLETKA - výučbová lekáreň
- Akreditovaný rozbor vody - Danum,s.r.o
- BEZ KONZERVANTOV DOMÁCE PRODUKTY
- Novinky
- Akcie a zľavy
Navštívené produkty
-
Mucosolvan long effect...
Tablety, tobolky.
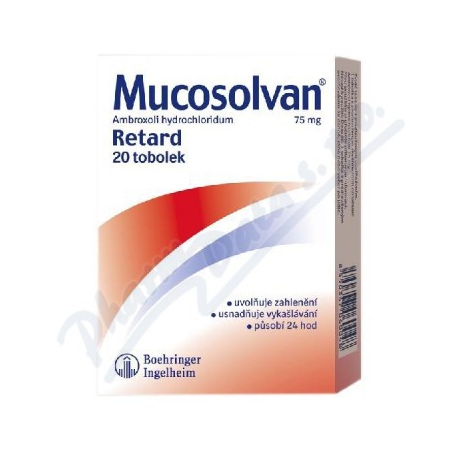
Mucosolvan long effect cps plg 20x75 mg
45329
Tablety, tobolky.
- Napíšte názor
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTI LIEKU
1. NÁZOV LIEKU
Mucosolvan Long effect
kapsuly s predĺženým uvoľňovaním
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
1 kapsula obsahuje 75 mg ambroxoliumchloridu
Úplný zoznam pomocných látok, pozri časť 6.1
3. LIEKOVÁ FORMA
kapsula s predĺženým uvoľňovaním
Podlhovasté tvrdé želatínové kapsuly, pozostávajúce z červeného nepriehľadného viečka a oranžového nepriehľadného tela, na viečku je biela potlač „MUC01“, na tele potlač symbolu spoločnosti Boehringer Ingelheim. Kapsuly obsahujú biely až takmer biely prášok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Sekretolytická liečba akútnych a chronických bronchopulmonálnych ochorení, sprevádzaných narušenou tvorbou väzkého prieduškového hlienu a jeho sťaženým transportom a vylučovaním.
4.2 Dávkovanie a spôsob podávania
Dospelí: 1 kapsula s predĺženým uvoľňovaním 1-krát denne.
Kapsuly sa nesmú otvárať ani žuvať, majú sa prehltnúť celé a zapiť dostatočným množstvom tekutiny. Zvyšky kapsúl, ktoré sú ojedinele prítomné v stolici, uvoľnili už liečivo počas prechodu tráviacim traktom a sú preto bezvýznamné.
MucosolvanRetard sa môže užívať s jedlom alebo bez jedla.
4.3 Kontraindikácie
Mucosolvan Retard nesmú užívať pacienti so známou precitlivenosťou na ambroxoliumchlorid alebo na iné zložky lieku.
V prípade zriedkavých dedičných ochorení, ktoré môžu viesť k neznášanlivosti pomocných látok lieku (pozri Osobitné upozornenia a opatrenia pri používaní) je podanie lieku kontraindikované.
4.4 Osobitné upozornenia a opatrenia pri používaní
V súvislosti s podávaním mukolytík ako je ambroxoliumchlorid sa veľmi zriedkavo vyskytli hlásenia o závažných kožných ochoreniach ako Stevensov-Johnsonov syndróm a toxická epidermálna nekrolýza (TEN). Vo väčšine prípadov sa dajú vysvetliť závažnosťou základného ochorenia a/alebo sprievodnou liečbou. Ešte v počiatočných fázach Stevensovho-Johnsonovho syndrómu alebo TEN môže pacient pociťovať nešpecifické príznaky chrípky ako predzvesť ochorenia, napr. horúčka, bolesť tela, rinitída, kašeľ a bolesť hrdla. Pri pomýlení si týchto príznakov s nešpecifickými príznakmi podobnými chrípke je možné, že sa už začalo s liečbou kašľa a prechladnutia. Preto, ak sa objavia nové lézie na pokožke alebo na sliznici, treba okamžite vyhľadať lekársku pomoc a predbežne treba liečbu ambroxoliumchloridom ukončiť.
V prípade renálnej insuficiencie alebo závažnej hepatopatie sa môže Mucosolvan Retard užívať len po konzultácii s lekárom. Tak ako pri iných liekoch metabolizovaných v pečeni renálnou elimináciou, pri závažnej renálnej insuficiencii sa dá očakávať prítomnosť naakumulovaných metabolitov ambroxoliumchloridu, ktoré sa vytvárajú v pečeni.
4.5 Liekové a iné interakcie
Neboli hlásené žiadne klinicky relevantné nežiaduce interakcie s inými liekmi.
4.6 Fertilita, gravidita a laktácia
Ambroxoliumchlorid prechádza placentárnou bariérou. Pri štúdiách na zvieratách sa nezistil priamy alebo nepriamy škodlivý vplyv na graviditu, embryonálny/fetálny vývoj, priebeh pôrodu alebo postnatálny vývoj.
Rozsiahle klinické pozorovania po 28. týždni tehotenstva nepreukázali žiadne škodlivé účinky na plod.
Napriek tomu sa musia dodržiavať bežné opatrenia týkajúce sa užívania liekov v tehotenstve. Užívanie lieku Mucosolvan Retard, hlavne počas prvého trimestra, sa neodporúča.
Ambroxoliumchlorid sa vylučuje do materského mlieka. Užívanie lieku Mucosolvan Retard sa neodporúča dojčiacim matkám, aj keď sa nepredpokladá výskyt nežiaducich účinkov u dojčených detí.
4.7. Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Nie sú údaje o ovplyvnení schopnosti viesť vozidlá a obsluhovať stroje. Neuskutočnili sa žiadne štúdie o účinkoch na schopnosť viesť vozidlá a obsluhovať stroje.
4.8. Nežiaduce účinky
Frekvencia podľa konvencií MedDRA:
Veľmi časté ≥1/10
Časté ≥1/100 až <1/10
Menej časté ≥1/1 000 až <1/100
Zriedkavé ≥1/10 000 až <1/1 000
Veľmi zriedkavé <1/10 000
Neznáme nedajú sa stanoviť z dostupných údajov
Poruchy gastrointestinálneho traktu
Časté: nevoľnosť (nauzea)
Menej časté: hnačka, vracanie, porucha trávenia, bolesť brucha
Poruchy kože a podkožného tkaniva
Zriedkavé: vyrážka, žihľavka
Veľmi zriedkavé: Stevensov-Johnsonov syndróm, toxická epidermálna nekrolýza (pozri časť 4.4)
Neznáme: angioedém (náhly opuch kože alebo slizníc, ktorý môže spôsobiť sťažené dýchanie), svrbenie
Poruchy imunitného systému
Neznáme: precitlivenosť, anafylaktické reakcie (rýchlo postupujúca, život ohrozujúca alergická reakcia) vrátane anafylaktického šoku (náhla, závažná a niekedy smrteľná alergická reakcia charakterizovaná sťaženým dýchaním, kolapsom obehového systému a náhlym opuchom)
4.9 Predávkovanie
Doposiaľ sa nezaznamenali žiadne špecifické príznaky predávkovania. Na základe doterajších skúseností a/alebo záznamov o náhodnom predávkovaní lieku boli príznaky predávkovania zhodné
so známymi vedľajšími účinkami, ktoré sa vyskytli pri odporučenom dávkovaní a môžu vyžadovať symptomatickú liečbu.
5. FARMAKOLOGICKÉ VLASNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: expektoranciá, mukolytiká, ATC kód: R05CB06
Predklinické štúdie ukázali, že ambroxoliumchlorid, liečivo lieku Mucosolvan Retard, zvyšuje vylučovanie hlienu z dýchacích ciest, zlepšuje tvorbu pľúcneho surfaktantu a stimuluje činnosť riasiniek. Toto pôsobenie vedie k zlepšeniu pohybu a transportu hlienu (mukociliárneho klírensu). Zlepšenie mukociliárneho klírensu bolo preukázané v klinických farmakologických štúdiách.
Zlepšenie exkrécie tekutín a mukociliárneho klírensu uľahčuje vykašliavanie a zmierňuje kašeľ.
Lokálny anestetický účinok ambroxoliumchloridu sa sledoval na modeli králičieho oka, čo je vysvetliteľné blokovacími vlastnosťami sodíkového kanála. In vitro bolo preukázané, že ambroxoliumchlorid blokuje klonované neurónové sodíkové kanály. Väzba bola reverzibilná a závisela od koncentrácie.
Zistilo sa, že vylučovanie cytokínu z krvi, ale aj z mononukleárnych a polymorfonukleárných buniek viazaných na tkanivo, bolo výrazne znížené pri in vitro ambroxoliumchloride.
V klinických sledovaniach bola u pacientov s bolesťou hrdla výrazne znížená bolesť hltana a sčervenanie.
Tieto farmakologické vlastnosti sú v súlade s doplnkovými pozorovaniami klinickej účinnosti liečby horných dýchacích ciest ambroxoliumchloridom, ktoré viedli k rýchlej úľave od bolesti a po inhalácii k poľaveniu ťažkostí súvisiacich s bolesťou v oblasti uší – nosa – priedušnice.
Súčasné užívanie ambroxoliumchloridu a antibiotík (amoxicilín, cefuroxim, erytromycín) vedie
ku zvyšovaniu koncentrácie antibiotík v bronchopulmonálnom sekréte a v spúte.
5.2 Farmakokinetické vlastnosti
Absorpcia
Absorpcia všetkých perorálnych foriem ambroxoliumchloridu bez oneskoreného uvoľňovania je rýchla a takmer kompletná, s linearitou dávky v terapeutickom rozmedzí. Maximálne plazmatické koncentrácie sa dosahujú počas 1 až 2,5 hodín po perorálnom podaní pri forme okamžitého uvoľňovania a priemerne po 6,5 hodinách pri forme pomalého uvoľňovania. Absolútna biodostupnosť po podaní 30 mg tablety bola 79 %. Kapsula s pomalým uvoľňovaním vykázala relatívnu dostupnosť 95 % (normalizovaná dávka) v porovnaní s dennou dávkou 60 mg (30 mg dvakrát denne) podávanej vo forme tabliet s okamžitým uvoľňovaním.
Distribúcia
Distribúcia ambroxoliumchloridu z krvi do orgánov je rýchla a výrazná, s maximálnou koncentráciou liečiva zistenou v pľúcach. Distribučný objem po perorálnom podaní lieku sa stanovil na 552 l. V terapeutickom rozmedzí bola zistená väzba na plazmatické bielkoviny približne 90 %.
Metabolizmus a vylučovanie
Približne 30 % perorálne podanej dávky sa eliminuje first-pass efektom. Ambroxoliumchlorid sa primárne metabolizuje v pečeni glukoronidáciou a premenou na kyselinu dibromo-antranilovú (približne 10 % z dávky) a na ďalšie menej významné metabolity. Štúdie na mikrozómoch ľudskej pečene ukázali, že CYP3A4 je zodpovedný za metabolizmus ambroxoliumchloridu na kyselinu dibromo-antranilovú.
Počas 3 dní po perorálnom podaní lieku sa približne 6 % dávky vyskytuje vo voľnej forme, pričom približne 26 % dávky sa metabolizuje v konjugovanej forme močom. Terminálny eliminačný polčas ambroxoliumchloridu je približne 10 hodín. Celkový klírens dosahuje hodnotu 660 ml/min, pričom renálny klírens predstavuje približne 8 % celkového klírensu.
Farmakokinetika u osobitných skupín populácie
U pacientov s hepatickou nedostatočnosťou je eliminácia ambroxoliumchloridu znížená, čo má
za následok približne 1,3 až 2-násobne vyššie plazmatické koncentrácie. Vzhľadom na vysoké terapeutické rozmedzie ambroxoliumchloridu nie je potrebná úprava dávkovania.
Iné
Nezistilo sa, že by vek a pohlavie ovplyvňovali farmakokinetiku ambroxoliumchloridu v klinicky relevantnom rozsahu, a preto nie je potrebná úprava dávkovacieho režimu.
Nezistilo sa, že jedlo ovplyvňuje biodostupnosť ambroxoliumchloridu.
5.3 Predklinické údaje o bezpečnosti
Ambroxoliumchlorid má veľmi nízku toxicitu.
V opakovaných štúdiách dávkovania, po podaní perorálnej dávky 150 mg/kg/deň (u myší 4 týždne), 50 mg/kg/deň (u potkanov 52 a 78 týždňov), 40 mg/kg/deň (u králikov 26 týždňov) a 10 mg/kg/deň
(u psov 52 týždňov) sa nepozorovali nežiaduce účinky (NOAEL), ani zreteľná orgánová toxicita.
Štúdie toxicity pri 4-týždňovom intravenóznom podávaní ambroxoliumchloridu u potkanov s dávkami 4,16 a 64 mg/kg/deň a u psov 45, 90 a 120 mg/kg/deň (infúzie 3 hod./deň) neupreukázali žiadnu závažnú lokálnu ani systémovú toxicitu vrátane histopatológie. Všetky nežiaduce účinky boli reverzibilné.
Ambroxoliumchlorid nevykazoval ani embryotoxický ani teratogénny účinok pri testovacích perorálnych dávkach do 3000 mg/kg/deň u potkanov a do 200 mg/kg/deň u králikov. Fertilita samčekov a samičiek potkanov nebola ovplyvnená pri dávkach do 500 mg/kg/deň.
NOAEL hodnota v štúdiách počas perinatálneho a postnatálneho vývoja bola 50 mg/kg/deň.
Dávka 500 mg/kg/deň ambroxoliumchloridu bola mierne toxická pre samičky a mláďatá, čo sa prejavilo zníženým prírastkom na hmotnosti a zníženým počtom mláďat.
Štúdie genotoxicity in vitro (Amesov test a test chromozomových mutácii) a in vivo (mikronukleový test na myšiach) neodhalil žiaden mutagénny potenciál ambroxoliumchloridu.
Ambroxoliumchlorid nevykazoval žiaden tumorogénny potenciál v štúdiách karcinogenity u myší
(50, 200 a 800 mg/kg/deň) a potkanov (65, 250 a 1 000 mg/kg/deň), ktorým sa podával spolu
s výživou počas 105, respektíve počas 116 týždňov.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Krospovidón CL
Karnaubský vosk
Stearylalkohol 97 %
Magnéziumstearát
6.2 Inkompatibility
Neaplikovateľné.
6.3 Čas použiteľnosti
3 roky
6.4 Špeciálne upozornenia a uchovávanie
Uchovávajte pri teplote do 30 ºC.
6.5 Druh obalu a obsah balenia
Vlastnosti a zloženie obalu: PVC/PVDC/hliníkový blister, papierová škatuľka, písomná informácia
pre používateľa
Veľkosť balenia: 10, 20, 50 alebo 100 kapsúl s predĺženým uvoľňovaním
Nie všetky veľkosti balenia musia byť uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Žiadne zvláštne požiadavky.
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Boehringer Ingelheim International GmbH
Ingelheim nad Rýnom
Nemecko
8. REGISTRAČNÉ ČÍSLO
52/0256/07-S
9. DÁTUM PRVEJ REGISTRÁCIE/PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 28.09.2007
Dátum posledného predĺženia:
10. DÁTUM REVÍZIE TEXTU
07/2012